C’è qualcosa di profondamente ironico nel fatto che gli animali che cerchiamo di scacciare dai nostri bagni potrebbero essere la chiave per rivoluzionare l’industria dei materiali. I ragni hanno sempre prodotto una delle fibre più resistenti del pianeta, ma ora la scienza ha fatto un passo oltre: ha creato la prima generazione di ragni geneticamente modificati che producono seta artificiale fluorescente. La ricerca dell’Università di Bayreuth non è solo un traguardo tecnico, è un cambio di paradigma che apre scenari inimmaginabili per medicina, aerospazio e molto altro.
Il primo esperimento CRISPR sui ragni della storia
Il professor Thomas Scheibel e il suo dottorando Edgardo Santiago-Rivera hanno scelto il Parasteatoda tepidariorum, un ragno domestico comune, per questo esperimento pionieristico. La sfida era duplice: questi aracnidi sono notoriamente cannibali e hanno un genoma complesso, caratteristiche che li hanno tenuti lontani dai laboratori di ricerca per anni.
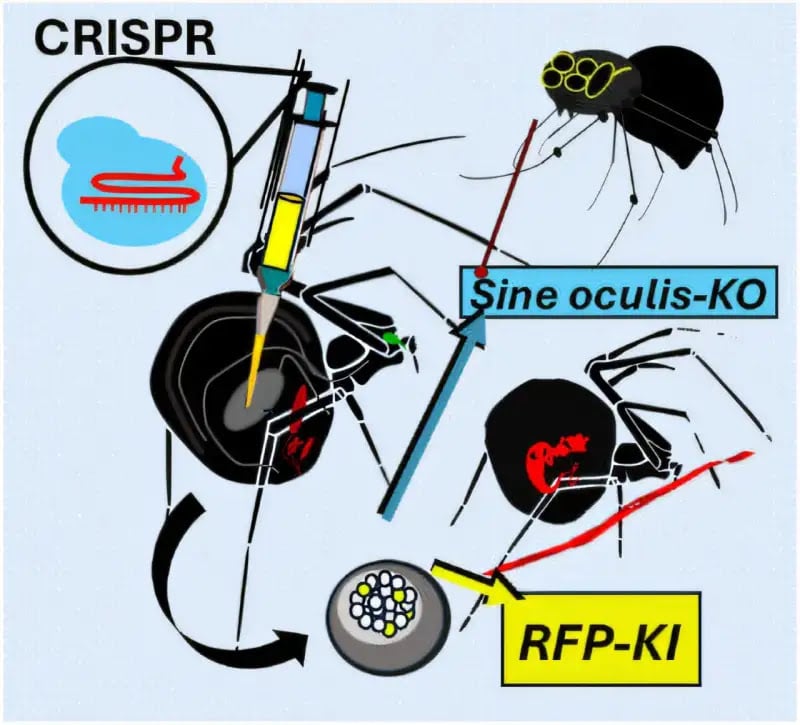
Per superare questi ostacoli, i ricercatori hanno sviluppato una soluzione iniettabile contenente i componenti del sistema CRISPR-Cas9 e una sequenza genetica per una proteina fluorescente rossa. Dopo aver anestetizzato i ragni con anidride carbonica, hanno iniettato la soluzione nelle uova non fecondate delle femmine. Il risultato? La prole ha prodotto seta artificiale con evidente fluorescenza rossa nella loro seta di trascinamento.
Perché modificare geneticamente i ragni per la seta artificiale
La domanda sorge spontanea: perché complicarsi la vita con i ragni quando esistono già metodi per produrre seta artificiale? La risposta sta nelle proprietà uniche di questo materiale naturale. La seta di ragno è estremamente resistente alla trazione, elastica, leggera e biodegradabile. Come abbiamo già sottolineato, le precedenti ricerche sulla seta artificiale avevano difficoltà a replicare completamente queste caratteristiche.
Applicazioni future della seta artificiale modificata
Questa seta artificiale fluorescente potrebbe trasformare diversi settori. In medicina, potrebbe essere utilizzata per suture biocompatibili e fili chirurgici avanzati. L’industria aerospaziale potrebbe sfruttarla per materiali compositi ultraleggeri e resistenti, mentre il settore tessile potrebbe finalmente avere un’alternativa sostenibile alle fibre sintetiche.
Il team ha dimostrato anche la tecnica del “knock-out” genetico, disattivando il gene sine oculis responsabile dello sviluppo degli occhi. I ragni risultanti, privi di organi visivi, hanno confermato il ruolo cruciale di questo gene, ampliando la comprensione genetica degli aracnidi.
La ricerca, pubblicata su Angewandte Chemie, rappresenta solo l’inizio. Scheibel sottolinea che questa proteina modificata potrebbe aumentare ulteriormente la resistenza alla trazione della seta artificiale, aprendo possibilità ancora inesplorate nel campo dei biomateriali del futuro.


