Funziona così: inspiri nanoparticelle (come quando uno usa un inalatore per l’asma), aspetti dieci minuti, poi espiri in un sensore grande quanto una moneta. Se i tuoi polmoni hanno un’infezione, gli enzimi della malattia tagliano dei biomarcatori sintetici attaccati alle nanoparticelle, che finiscono nel respiro. Il sensore li cattura con molecole d’acqua e li identifica usando la luce. Tutto qui: fine delle radiografie e delle attese. Si chiama PlasmoSniff, è un prototipo del MIT, e funziona. Sui topi, per ora.
Come fa un chip a leggere il respiro
Il progetto nasce dall’incontro tra due gruppi di ricerca del MIT. Da una parte Loza Tadesse, ingegnera meccanica specializzata in spettroscopia e dispositivi diagnostici portatili. Dall’altra Sangeeta Bhatia, che da anni sviluppa nanoparticelle “intelligenti”: particelle microscopiche dotate di biomarcatori sintetici progettati per staccarsi solo in presenza di enzimi specifici, le proteasi, prodotte da determinate malattie.
Il principio era già stato dimostrato nel 2020: il gruppo di Bhatia aveva rilevato biomarcatori della polmonite nel respiro di topi infetti, a concentrazioni bassissime (circa 10 parti per miliardo). Il problema era lo strumento usato per farlo: uno spettrometro di massa, un macchinario ingombrante e costosissimo, tutt’altro che portatile.
Insomma: sapevano cosa cercare nel respiro. Mancava un modo pratico per farlo.
L’oro che ascolta le molecole
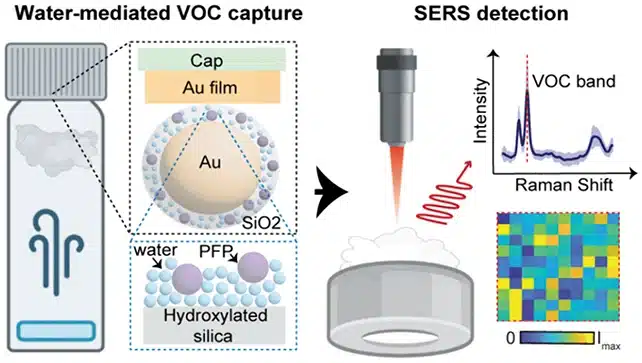
La soluzione si chiama plasmonica: lo studio di come la luce interagisce con la materia su scala nanometrica. Il cuore di PlasmoSniff è un film sottile d’oro, sopra il quale sono sospese nanoparticelle d’oro rivestite di silice porosa. Tra le particelle e il film si crea un’intercapedine di appena 5 nanometri, meno di un centesimo del diametro di un capello umano.
Ecco, quel vuoto minuscolo è dove succede tutto. La silice è modificata per legarsi con l’acqua, e l’acqua a sua volta intrappola i biomarcatori esalati: è una specie di “velcro” molecolare che trattiene solo le particelle giuste. Una volta catturati, i biomarcatori vengono illuminati con un laser e identificati tramite la spettroscopia Raman, una tecnica che misura le vibrazioni delle molecole e ne riconosce la loro “impronta digitale” chimica.
Il segnale, normalmente debolissimo, viene amplificato dalla risonanza plasmonica dell’oro: gli elettroni nella struttura oscillano collettivamente in risposta alla luce, concentrando il campo elettromagnetico nell’intercapedine e rendendo visibile ciò che normalmente sarebbe invisibile.
Scheda studio
Titolo: Toward breath-based diagnostics via water-mediated capture of synthetic breath biomarkers in SERS-active plasmonic nanogaps
Autori: Aditya Garg, Morales M., Shah A. et al.
Istituzione: Massachusetts Institute of Technology (MIT)
Rivista: Nano Letters, febbraio 2026
DOI: 10.1021/acs.nanolett.5c05948
Il respiro come esame clinico (ma non ancora)
Il test è stato condotto su fluido polmonare di topi sani, arricchito con biomarcatori della polmonite e poi fatto evaporare per simulare il respiro. Il sensore, montato sul tappo della fiala, ha rilevato i biomarcatori a concentrazioni clinicamente rilevanti: nessun essere umano ha ancora soffiato in PlasmoSniff.
Il passo successivo è costruire un sistema di raccolta del respiro: una maschera collegata al sensore in cui il paziente respira per circa cinque minuti, combinata con uno spettrometro Raman portatile.
Attenzione, però: siamo ancora nella fase in cui il sensore riconosce un solo biomarcatore, in condizioni controllate, senza la complessità del respiro umano reale (che contiene centinaia di composti organici volatili). Il passaggio ai test clinici richiederà tempo, e la certificazione medica ancora di più.
Un naso per tutto
La cosa interessante è che PlasmoSniff non è pensato solo per la polmonite. Il team del MIT sostiene che la piattaforma può essere adattata a qualsiasi malattia le cui proteasi producano biomarcatori con un'”impronta vibrazionale” nota: tumori, infezioni intestinali, virus. E anche ad applicazioni non mediche: rilevamento di inquinanti atmosferici, sostanze chimiche industriali, qualsiasi molecola capace di formare legami a idrogeno con l’acqua.
Un cane da tartufo universale, ma grande quanto un’unghia e fatto d’oro.
La strada dai topi alle cliniche è lunga (e costosa, e piena di sorprese regolatorie). Ma il principio è elegante: trasformare il respiro da sottoprodotto biologico a fonte di informazione diagnostica, usando la luce per leggere ciò che i polmoni raccontano.
Resta da vedere se il racconto, una volta ascoltato negli esseri umani, sarà altrettanto chiaro.
Approfondisci
L’idea di usare il respiro come strumento diagnostico non è nuova, ma sta accelerando. Ne abbiamo parlato a proposito del sensore nanotecnologico che rileva il cancro al polmone dall’isoprene esalato, e anche della diagnosi vocale di malattie respiratorie tramite smartphone sviluppata da VoiceMed. A monte di tutto c’è il mondo dei biosensori a nanoparticelle, di cui avevamo esplorato le potenzialità diagnostiche già nel 2021.