Il chip è grande come una scheda microSIM tagliata a metà. Spesso quanto un capello. Lo inseriscono sotto la retina in un’ora e mezza, poi aspettano un mese che l’occhio si abitui all’impianto retinico. Quando accendono gli occhiali per la prima volta, qualcuno piange. Altri restano in silenzio, fissando una lettera che non vedevano da anni. Sheila Irvine, paziente britannica, descriveva la sua cecità come “due dischi neri davanti agli occhi”. Ora legge di nuovo. Non perfettamente: bianco e nero, sfocato, campo visivo ridotto. Ma legge.
Lo studio pubblicato sul New England Journal of Medicine conferma quello che 27 pazienti su 32 stanno già sperimentando: un impianto retinico fotovoltaico può ridare la vista a chi l’ha persa per degenerazione maculare avanzata.
Come funziona l’impianto retinico PRIMA
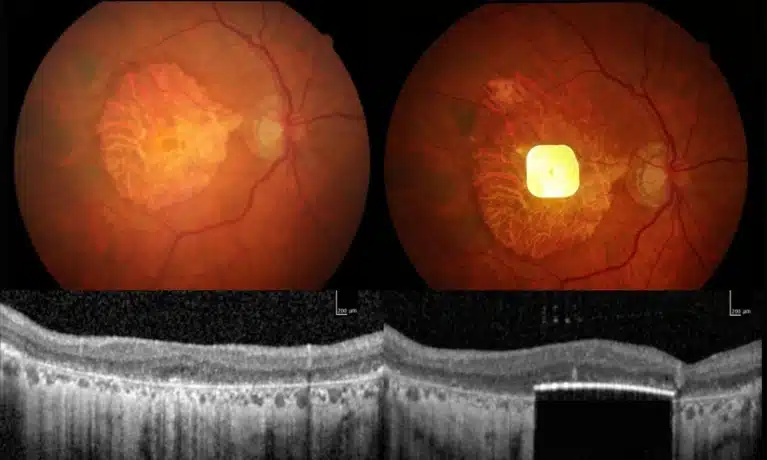
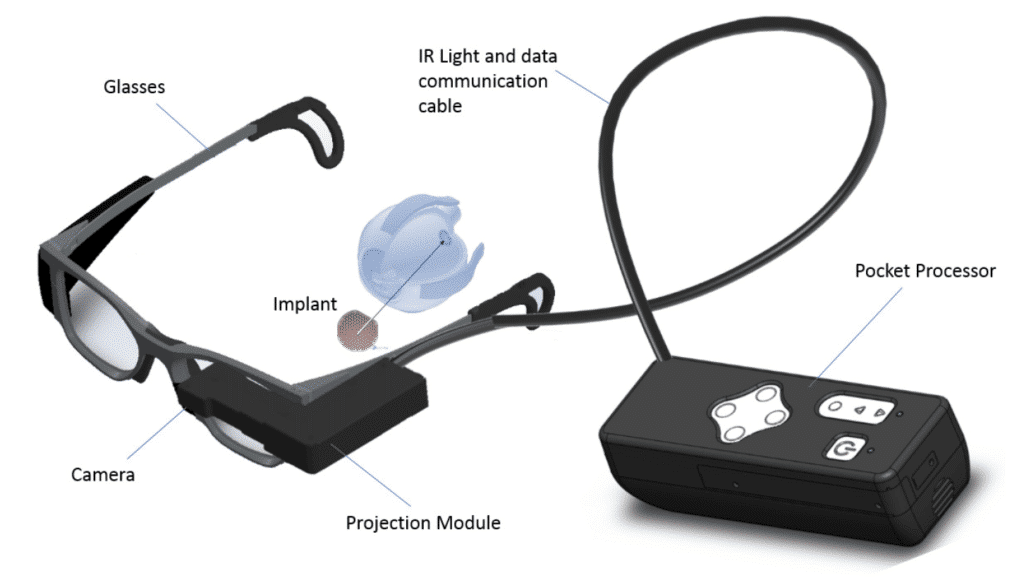
Il dispositivo si chiama P.R.I.M.A (Photovoltaic Retina Implant Micro Array) ed è frutto di vent’anni di ricerche condotte dal fisico Daniel Palanker della Stanford University. Un quadratino wireless di 2 millimetri per lato, spesso appena 30 micrometri, viene impiantato chirurgicamente sotto la retina centrale attraverso una vitrectomia. Niente cavi, niente batterie esterne. Il chip ospita 378 pixel fotosensibili disposti a nido d’ape che funzionano come un pannello solare microscopico.
Ma il chip da solo non basta. Serve un paio di occhiali speciali dotati di videocamera frontale e proiettore a infrarossi. La videocamera cattura le scene visive, il computer tascabile (che il paziente indossa alla cintura) le elabora, e il proiettore le trasforma in schemi di luce infrarossa che vengono sparati direttamente sul chip impiantato. Quando la luce colpisce i pixel, questi generano impulsi elettrici che stimolano i neuroni retinici sopravvissuti, bypassando completamente i fotorecettori morti. Le informazioni viaggiano poi attraverso il nervo ottico fino al cervello, che le interpreta come immagini.
È come un sistema di traduzione simultanea: la realtà esterna viene convertita in infrarosso, l’infrarosso in elettricità, l’elettricità in segnali neurali. Tre passaggi per aggirare il guasto biologico.
Impianto retinico, lo studio europeo che cambia tutto
Lo studio clinico PRIMAvera ha coinvolto 38 pazienti ultrasessantenni in 17 ospedali distribuiti tra Francia, Germania, Italia, Paesi Bassi e Regno Unito. Tutti affetti da atrofia geografica, la forma più grave di degenerazione maculare legata all’età: i fotorecettori al centro della retina morti, la visione centrale azzerata, solo un sottile bordo di visione periferica sopravvissuto.
Coordinato da Frank Holz dell’Università di Bonn, il trial ha prodotto numeri che parlano chiaro. Dei 32 pazienti che hanno completato dodici mesi di monitoraggio, l’81% ha ottenuto miglioramenti clinicamente rilevanti nell’acuità visiva. In media, chi ha ricevuto l’impianto retinico è riuscito a leggere cinque righe in più sulla tabella optometrica standard. Alcuni pazienti, che prima dell’intervento non riuscivano nemmeno a distinguere la presenza della tabella, hanno recuperato una capacità di lettura sorprendente.
Mahi Muqit, professore presso l’UCL Institute of Ophthalmology e consulente del Moorfields Eye Hospital di Londra, ha guidato la sezione britannica dello studio. “Nella storia della visione artificiale, questo rappresenta una nuova era”, ha dichiarato.
“I pazienti ciechi riescono effettivamente a recuperare una visione centrale significativa, cosa mai realizzata prima.”
Cosa vedono davvero i pazienti
Non è visione normale. Le immagini appaiono in bianco e nero con una tinta giallastra, sfocate, con un campo visivo ridotto. La risoluzione attuale permette di distinguere forme, contrasti, movimenti. Leggere è possibile, come detto, anche se lentamente. Gli occhiali hanno una funzione zoom per ingrandire i testi e regolare il contrasto. Alcuni pazienti descrivono l’esperienza come “vedere attraverso una finestra stretta”.
Sheila Irvine, la paziente di cui vi parlavo a inizio articolo, ha raccontato che più ore dedica all’uso del dispositivo, più cose riesce a fare: leggere le etichette sui barattoli, completare le parole crociate, immergersi nuovamente nella lettura. Certo, il processo richiede mesi di riabilitazione intensiva. Il cervello deve imparare a interpretare segnali visivi completamente nuovi, tipo un musicista che passa dal pianoforte alla batteria: le note sono sempre quelle, ma lo strumento funziona diversamente.
Come vi dicevo già a novembre 2024, i primi risultati del chip PRIMA stavano mostrando segnali promettenti. Ora i dati confermano: funziona.
Quando sarà disponibile l’impianto retinico
Science Corporation, l’azienda californiana che ha acquisito la tecnologia dalla francese Pixium Vision dopo il suo fallimento nel 2024, ha presentato a giugno 2025 la richiesta di certificazione CE per il mercato europeo. Se approvato, il dispositivo potrebbe essere disponibile entro il 2026. Negli Stati Uniti sono già in corso trattative con la Food and Drug Administration.
Palanker ha già sviluppato una versione migliorata del chip con risoluzione superiore, attualmente in fase di test sugli animali. Più pixel, immagini più nitide, campo visivo ampliato. La tecnologia sta progredendo rapidamente.
Ma ci sono limiti. Come sottolineato da Nurse Times, l’intervento ha prodotto “eventi avversi” nel 95% dei casi: aumento della pressione oculare, lacerazioni retiniche, sanguinamenti. Problemi gestibili e risolti entro due mesi nella maggioranza dei pazienti, ma non banali.
Il candidato ideale è chi ha perso completamente la vista centrale per degenerazione maculare secca, senza altre patologie oculari, e ha sviluppato una vista significativa in giovane età. Una fetta purtroppo ancora ristretta dei 5 milioni di persone al mondo affette da questa condizione.
Impiango retinico, la lunga marcia della vista artificiale
Vent’anni di ricerche per arrivare a una visione sfocata in bianco e nero. Sembra poco. Ma per chi viveva con due dischi neri davanti agli occhi, distinguere una lettera è un evento cosmico. La tecnologia non ripristina ciò che si è perso: costruisce qualcosa di nuovo, diverso, ibrido. Non è l’occhio biologico che riprende a funzionare. È un sistema elettronico che parla la lingua del cervello.
E forse è proprio questo il punto. Non stiamo “riparando” la vista. Stiamo inventando un altro modo di vedere.


