Un foglio sottile come carta si avvolge attorno a un nervo. Comincia a scaldarsi. Non brucia, arriva giusto a 43 gradi, la temperatura di una giornata torrida. Il nervo smette di trasmettere segnali: il dolore si ferma. Dopo qualche settimana il dispositivo si dissolve da solo, come una pastiglia effervescente nell’acqua. Non serve toglierlo con un altro intervento. Semplicemente sparisce.
È quello che hanno sviluppato i ricercatori della Northwestern University: un impianto bioassorbibile che blocca il dolore usando il calore invece dei farmaci. Niente oppioidi, niente fili che escono dalla pelle, niente batterie da cambiare. Solo calore controllato che mette in pausa i nervi quando serve.
Come bloccare il dolore senza farmaci
Il team di ricercatori ha pubblicato su Advanced Functional Materials i dettagli di un dispositivo bioassorbibile che gestisce il dolore attraverso il calore controllato. Non è la prima volta che qualcuno prova a usare la temperatura per interferire con la trasmissione nervosa. Ve ne abbiamo parlato 3 anni fa: nel 2022 lo stesso gruppo aveva sviluppato un sistema di raffreddamento che bloccava il dolore portando i nervi sotto i 10 gradi. Funzionava, ma il freddo estremo richiedeva controlli precisi per evitare danni ai tessuti.
Il calore lavora all’opposto. Tra 42 e 45 gradi Celsius, i canali ionici delle cellule nervose diventano meno efficienti. Il sodio e il potassio faticano a entrare e uscire dalle membrane. Le onde elettriche che portano i segnali di dolore lungo l’assone rallentano, si affievoliscono, alla fine si bloccano. Non è una distruzione. È un’interferenza temporanea. Quando la temperatura torna normale, il nervo riprende a funzionare come prima.
I test su modelli animali hanno mostrato che il dispositivo raggiunge la temperatura target in 30 secondi e mantiene 43,5 °C con variazioni minime di ±0,3 gradi.
Dopo 4 minuti di riscaldamento, i segnali nervosi cominciano a indebolirsi. A 5 minuti, il blocco è completo.
Spegnendo il riscaldatore, la trasmissione nervosa torna normale entro pochi minuti.
Oro, silicio e polimeri che scompaiono
L’impianto è costruito a strati. Due elementi funzionali serpeggianti in oro ultrasottile: uno scalda quando la corrente lo attraversa, l’altro misura la temperatura locale. Un isolante in biossido di silicio (500 nanometri) separa i circuiti. Il tutto è racchiuso in polimeri bioassorbibili. Al momento i test comprendono due opzioni: polianidride, che si dissolve in una settimana circa, e fibroina di seta rigenerata e plastificata con glicerolo, che dura fino a 14 giorni.
Il dispositivo non contiene batterie. L’energia arriva dall’esterno tramite bobine wireless che operano a 13,56 MHz, la stessa frequenza usata per le carte contactless. Il segnale attraversa pelle e tessuti senza problemi fino a 6 millimetri di profondità. Un regolatore di tensione interno impedisce al sistema di surriscaldarsi se l’alimentazione esterna aumenta improvvisamente.
Il sensore di temperatura chiude il cerchio. Legge continuamente i gradi del tessuto nervoso e regola la potenza del riscaldatore. Questa retroazione automatica mantiene l’impianto nella finestra terapeutica (42-45 °C) senza intervento umano continuo. Nei test, il sistema è rimasto stabile per oltre 20.000 cicli di flessione e torsione, simulando il movimento costante dei tessuti corporei.
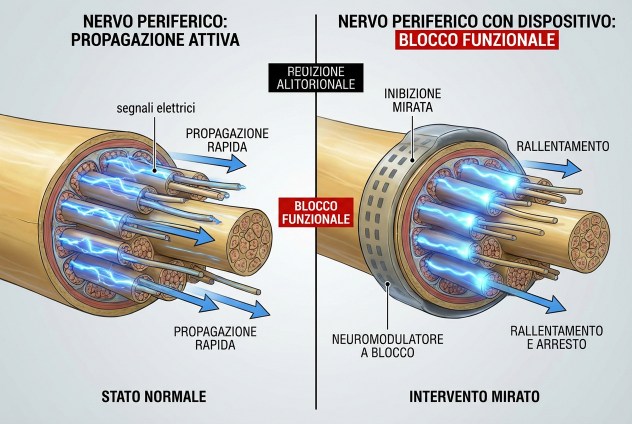
Perché il calore funziona meglio del freddo contro il dolore
Il blocco termico del dolore non è nuovo nella pratica medica. Il calore viene usato da decenni in fisioterapia per rilassare muscoli contratti o alleviare rigidità articolare. Ma applicare calore in modo così preciso, su un singolo nervo periferico, con controllo al decimo di grado, è un’altra storia.
Il vantaggio del calore rispetto al freddo sta nella finestra di sicurezza più ampia. Temperature sotto i 10 gradi possono causare danni da congelamento se mantenute troppo a lungo. Il margine di errore è stretto. Con il calore, la zona sicura si estende tra i 42 e i 45 gradi: tre gradi pieni di manovra prima che comincino problemi seri. Sopra i 45 gradi per periodi prolungati, i tessuti subiscono danni irreversibili. Ma il sensore integrato e il controllo automatico mantengono il dispositivo ben sotto questa soglia critica.
Gli oppioidi bloccano il dolore interferendo con i recettori nel cervello e nel midollo spinale. Funzionano, ma innescano dipendenza fisica, tolleranza crescente, e una lunga lista di effetti collaterali che vanno dalla costipazione alla depressione respiratoria. Gli anestetici locali diffondono nei tessuti circostanti e perdono efficacia dopo poche ore. Il blocco termico lavora localmente, su un nervo specifico, senza molecole che si distribuiscono nel corpo.
Il dato più rilevante? In ratti con nervi sciatici stimolati elettricamente, l’attivazione del riscaldatore ha ridotto progressivamente l’ampiezza dei potenziali d’azione composti fino alla soppressione completa.
Spegnendo il dispositivo, la conduzione nervosa è tornata ai livelli basali senza evidenze di danno permanente nei tessuti analizzati istologicamente.
Quando serve un impianto che sparisce
Il dolore acuto post-operatorio rappresenta il campo d’azione immediato. Una persona subisce un intervento chirurgico. Il chirurgo posiziona l’impianto sul nervo che innerva l’area operata. Per giorni o settimane, il dispositivo blocca il dolore mentre i tessuti guariscono. Poi si dissolve. Niente secondo intervento per rimuoverlo. Niente fili esterni che possono infettarsi. Niente hardware permanente nel corpo.
L’idea non è sostituire completamente gli antidolorifici. È ridurne il carico. Meno morfina significa meno nausea, meno sedazione, meno rischio di dipendenza. Per pazienti che escono da amputazioni, mastectomie, ricostruzioni articolari, questo può fare la differenza tra una ripresa funzionale e settimane di torpore chimico.
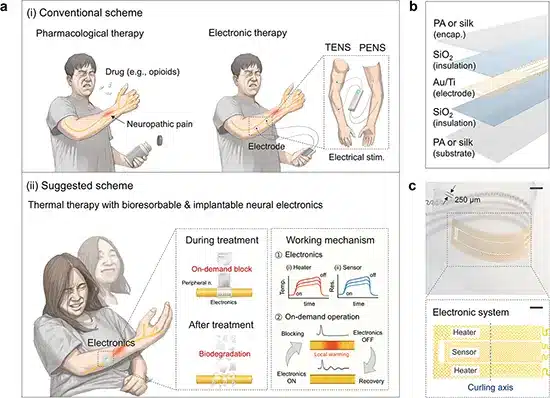
Ci sono ancora dei limiti
Il primo, così ci capiamo subito: l’oro si dissolve, ma non svanisce nel nulla. Ogni impianto lascia tracce microscopiche di metallo nei tessuti: le quantità sono minime (113 microgrammi), ma non zero. Certo, l’oro è biocompatibile e viene usato da decenni in dispositivi medici, quindi il rischio è considerato trascurabile. Ma non è un sistema completamente “invisibile” dopo la dissoluzione.
Ancora: l’alimentazione wireless funziona fino a 6 millimetri di profondità. Per nervi più profondi serve aumentare la potenza del trasmettitore esterno, con limiti dettati dalla sicurezza dei tessuti circostanti esposti al campo elettromagnetico. E il controllo della temperatura, per quanto preciso, dipende dal corretto posizionamento del sensore sul nervo. Un millimetro di distanza può significare letture imprecise. Ci stanno lavorando.
Dal laboratorio al corpo umano, i prossimi passi anti dolore
I prossimi sviluppi puntano a sostituire le tracce d’oro con metalli completamente bioassorbibili. Molibdeno, tungsteno, ferro: materiali che si dissolvono lentamente ma completamente, senza residui permanenti. Il problema è mantenere conducibilità elettrica e resistenza meccanica sufficienti per il tempo necessario.
Un altro fronte riguarda l’estensione dell’autonomia. I polimeri attuali durano al massimo due settimane. Per alcune applicazioni può bastare. Per altre serve di più. Modificare la cristallinità della fibroina di seta cambiando il contenuto di glicerolo allunga i tempi di degradazione, ma c’è un compromesso con la flessibilità meccanica del dispositivo.
Gli stimolatori nervosi impiantabili esistono già, ma sono permanenti o semipermanenti.
Richiedono interventi chirurgici per l’impianto e per la rimozione. Generano cicatrici. Possono infettarsi. I fili che attraversano la pelle rappresentano vie d’ingresso per batteri. Ogni connessione fisica è un punto di vulnerabilità.
Un impianto temporaneo che agisce quando serve e poi scompare ribalta questa logica. Non è perfetto. Non sostituirà tutti i metodi di gestione del dolore. Ma occupa uno spazio che prima era vuoto: il blocco nervoso selettivo, reversibile, senza innesti permanenti.
Il dispositivo pesa meno di un decimo di milligrammo. Scalda un nervo fino a farlo tacere. Poi si scioglie come neve al sole. Resta da vedere se il corpo umano, con la sua complessità maggiore rispetto ai modelli animali, reagirà nello stesso modo prevedibile. Ma il principio è solido: calore controllato, posizione precisa, dissoluzione programmata.
Tra cinque anni questi impianti potrebbero uscire dalle sale operatorie avvolti attorno ai nervi di pazienti reali. Oppure no. La strada dalla prova di concetto alla clinica è piena di ostacoli imprevisti.
Per ora resta un foglio d’oro sottile che riscalda e sparisce. Quasi.


