In Italia ci sono circa mille persone in lista d’attesa per un trapianto di fegato. L’attesa media, per chi non è in urgenza, è un anno e sette mesi. Per molti è troppo: alcuni si ammalano troppo gravemente per affrontare un’operazione di otto-dieci ore, altri purtroppo non arrivano in tempo. Negli Stati Uniti, invece, i pazienti in lista sono oltre diecimila. Il problema, ovunque, è sempre lo stesso: gli organi disponibili sono pochi, le persone che ne hanno bisogno sono tante, e il trapianto è un intervento pesantissimo. Ecco, è da qui che parte la storia dei mini fegati: dall’idea che forse non serve sostituire l’organo malato per intero. Forse basta affiancargli un aiutante.
Cosa sono questi mini fegati, spiegato semplice
Il fegato fa più o meno cinquecento cose diverse: produce proteine, smaltisce farmaci, regola la coagulazione del sangue, ripulisce dai batteri a tanto, tanto altro. La maggior parte di questo lavoro lo fanno le cellule chiamate epatociti: sono loro le operaie del fegato. E sono anche il punto di partenza dei ricercatori del MIT.
Da anni gli scienziati provano a iniettare epatociti nei pazienti, sperando che si attacchino da qualche parte e ricomincino a lavorare. Il problema è che le cellule, da sole, sono fragili: appena entrano nel corpo non trovano un posto stabile, non si collegano ai vasi sanguigni, non ricevono nutrimento e muoiono nel giro di poco. È un po’ come trapiantare una piantina senza terra né acqua: per quanto sia sana, non sopravvive.
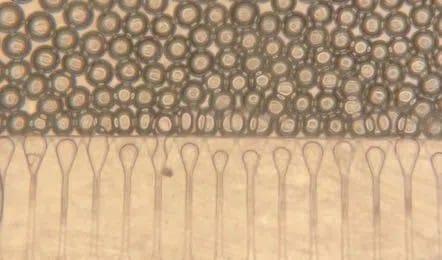
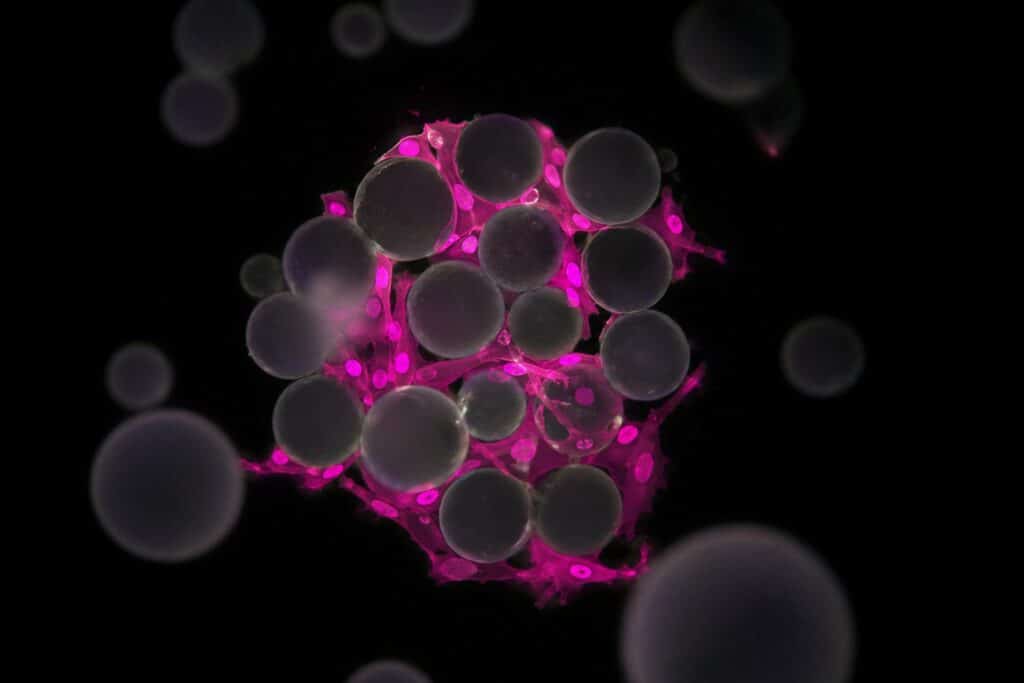
Il team guidato da Sangeeta Bhatia e Vardhman Kumar ha avuto l’idea di darle una casa. Hanno costruito delle micro-sferette di idrogel (un materiale gelatinoso, biocompatibile, che il corpo tollera bene) e ci hanno mescolato dentro le cellule del fegato. Il risultato è un liquido lattiginoso che ha una proprietà sorprendente: quando viene spinto attraverso un ago, si comporta come un fluido, scorre. Appena entra nel corpo e la pressione finisce, le sferette si bloccano una contro l’altra e formano una specie di impalcatura solida. Le cellule restano lì, protette, e il corpo intorno comincia a far crescere nuovi vasi sanguigni che le raggiungono.
Nel giro di pochi giorni quella soluzione iniettata diventa un piccolo tessuto vivo, collegato alla circolazione del paziente: un mini fegato funzionante. Io davanti a queste cose resto sempre meravigliato.
Scheda studio
Titolo: Image-guided injectable niche for hepatocyte transplantation
Autori principali: Vardhman Kumar, Sangeeta N. Bhatia (MIT)
Rivista: Cell Biomaterials (marzo 2026)
Risultato chiave: nei topi, le cellule iniettate sono rimaste vitali e funzionanti per otto settimane (durata totale dello studio), producendo proteine ed enzimi tipici del fegato.
Sede dell’iniezione: tessuto adiposo addominale, non vicino al fegato malato.
Componenti dell’iniezione: epatociti umani primari + fibroblasti (cellule “di supporto”) + microsfere di idrogel.
Il dettaglio che cambia tutto: non serve mettere il mini fegato vicino al fegato
Questa è la parte sorprendente, e vale la pena fermarsi un secondo. Il fegato è un organo complicato, attaccato in profondità all’addome, vicino a vasi sanguigni grossi e delicati. Operarlo è difficile, anche solo per appoggiargli accanto qualcosa.
Bhatia e Kumar hanno scoperto che non serve farlo. Hanno iniettato il mini fegato nel grasso della pancia (in una zona chiamata tessuto adiposo perigonadico), lontano dal fegato vero, e ha funzionato lo stesso. Le cellule hanno continuato a fare il loro mestiere, producendo le proteine giuste, come se fossero nel posto “sbagliato” ma non se ne fossero accorte. Kumar lo dice esplicitamente: per la stragrande maggioranza delle malattie del fegato, il graft non ha bisogno di stare attaccato all’organo originale.
Tradotto: significa che un giorno questa terapia potrebbe arrivare con una siringa nello studio del medico, non in una sala operatoria. È la differenza fra una giornata in day hospital e un ricovero di due settimane.
A cosa serve davvero, in pratica
Tre scenari concreti, in ordine di plausibilità.
Primo: il ponte verso il trapianto. Chi è in lista d’attesa con un fegato che non regge più ha un problema doppio: peggiora ogni giorno e ogni giorno ha meno chance di sopravvivere all’intervento quando finalmente arriva l’organo. Un mini fegato iniettato potrebbe tenerlo stabile, dargli giorni o mesi di funzionalità in più. Tradotto in vite, sono persone che oggi non ce la fanno e che domani potrebbero farcela.
Secondo: i pazienti che il trapianto non possono nemmeno fare. Ce ne sono tanti: troppo deboli, troppo anziani, con altre malattie che rendono l’operazione un rischio inaccettabile. Per loro oggi non c’è niente. Una terapia iniettabile, ripetibile, senza chirurgia, sarebbe una porta che oggi è chiusa.
Terzo: malattie genetiche del fegato. Alcune patologie ereditarie dipendono da una singola proteina che il fegato non sa più produrre. Non serve sostituire tutto l’organo: bastano abbastanza cellule giuste da fare quella proteina specifica. È esattamente quello che un mini fegato satellite potrebbe fornire, magari con cellule ingegnerizzate ad hoc.
L’idea di curare il fegato con un’iniezione si incrocia con altre linee di ricerca che stanno andando nella stessa direzione, dalle terapie genetiche che agiscono direttamente sulle cellule epatiche ai farmaci che invertono il danno della steatosi epatica. È un fronte che si muove, in più direzioni contemporaneamente.
Quello che ancora non funziona
Ora, come faccio sempre, metto i pesi sull’altro piatto della bilancia, perché vanno detti.
Anzitutto, il disclaimer di sempre: lo studio è sui topi, non sugli umani. O meglio: le cellule sono umane, l’ospite no: seguiranno il passaggio successivo (sui primati) e poi trial clinici: processi che richiedono anni. Le cellule sono rimaste attive per due mesi, ma due mesi è la durata dello studio, non un limite tecnico accertato: potrebbero durare di più, o di meno. Non lo sappiamo ancora.
Poi c’è la questione degli immunosoppressori. Le cellule di donatore vengono riconosciute come estranee e attaccate dal sistema immunitario, quindi il paziente dovrebbe prendere farmaci che gli abbassano le difese (con tutti gli effetti collaterali del caso, dalle infezioni più frequenti al rischio aumentato di certi tumori). Bhatia e il suo team stanno lavorando a cellule “stealth”, invisibili al sistema immunitario, ma siamo nel terreno delle cose che si stanno provando, non di quelle pronte.
C’è infine la concorrenza. Una società chiamata LyGenesis sta seguendo una strada parallela: far crescere mini-fegati nei linfonodi, però lei è già arrivata ai trial clinici sull’uomo. Approccio diverso, più invasivo, ma più avanti. Non si capisce ancora chi vincerà la corsa, o se vinceranno entrambi su pazienti diversi.
Quando lo vedremo davvero
Orizzonte stimato: 8-12 anni per le prime applicazioni nell’uomo, forse di più per la diffusione vera.
Servono trial clinici di Fase 1, 2 e 3 (di solito sette-dieci anni in tutto, se va bene), bisogna risolvere il nodo degli immunosoppressori e capire se le cellule “stealth” funzionano davvero. Poi serve un sistema produttivo: epatociti umani di qualità, in quantità industriali, lotti uniformi, costo sostenibile. I primi a beneficiarne saranno probabilmente i pazienti più gravi (urgenze nazionali, malattie genetiche rare), in centri ospedalieri specializzati e in Paesi ricchi. Solo dopo, forse, l’accesso si allargherà. Il fattore decisivo, alla fine, non sarà la chimica: sarà il prezzo.
Perché questa storia è bella, oltre che utile
C’è un dettaglio nel modo in cui questi mini fegati si formano che, raccontato bene, fa pensare. Le sferette di idrogel non sono un trucco da laboratorio: sono un esempio quasi poetico di come si possa lavorare con il corpo, non contro. Il corpo riconosce lo spazio fra una sferetta e l’altra come un posto in cui può crescere tessuto nuovo, e ci manda i suoi vasi sanguigni a farlo. La medicina del futuro, probabilmente, sarà fatta di tante cose così: non protesi che sostituiscono, ma materiali che invitano il corpo a ripararsi.
Vedere una soluzione lattiginosa entrare in una siringa e poi diventare, dentro al corpo, un piccolo organo che lavora ha qualcosa di stupefacente. Non per i fuochi d’artificio della scienza, ma per la semplicità del gesto: una puntura. Quella che oggi è un’operazione di otto ore, fra qualche anno, forse, sarà un appuntamento ambulatoriale.
Per quei mille italiani in lista d’attesa, e per tutti quelli che oggi nemmeno arrivano in lista perché troppo fragili, è il tipo di notizia che vale la pena tenere d’occhio.
I topi sono solo l’inizio. Ma stavolta, forse, l’inizio porta da qualche parte.