I topi non avrebbero dovuto vederla: nessun mammifero, in teoria, vede la luce infrarossa. Eppure hanno cominciato a leccare in attesa dell’acqua ogni volta che la luce invisibile si accendeva. E hanno imparato a percepire qualcosa che la natura non aveva mai dato loro.
L’esperimento è uscito su Nature Electronics, firmato da un gruppo della Yonsei University guidato dal professor Park Jang-ung. La domanda di partenza era classica: come restituire una qualche forma di vista a chi l’ha persa per malattie come la retinite pigmentosa o la degenerazione maculare? La risposta, quella, è meno classica.
Una retina artificiale che lavora dove i fotorecettori sono morti
Nelle malattie degenerative della retina, le prime cellule a cedere sono i fotorecettori, quelle che catturano la luce. Le cellule gangliari, che trasmettono il segnale al cervello attraverso il nervo ottico, spesso resistono. Le protesi retiniche puntano lì: stimolare quello che è rimasto in piedi, saltando quello che non c’è più.
Il dispositivo coreano fa esattamente questo, ma con due differenze sostanziali. La prima è che non lavora sulla luce visibile. Lavora sull’infrarosso vicino. La seconda è la sua morfologia: è soffice. Non rigido, non metallico nel senso classico. Il contatto con il tessuto retinico è meno traumatico di quanto succede con gli impianti tradizionali.

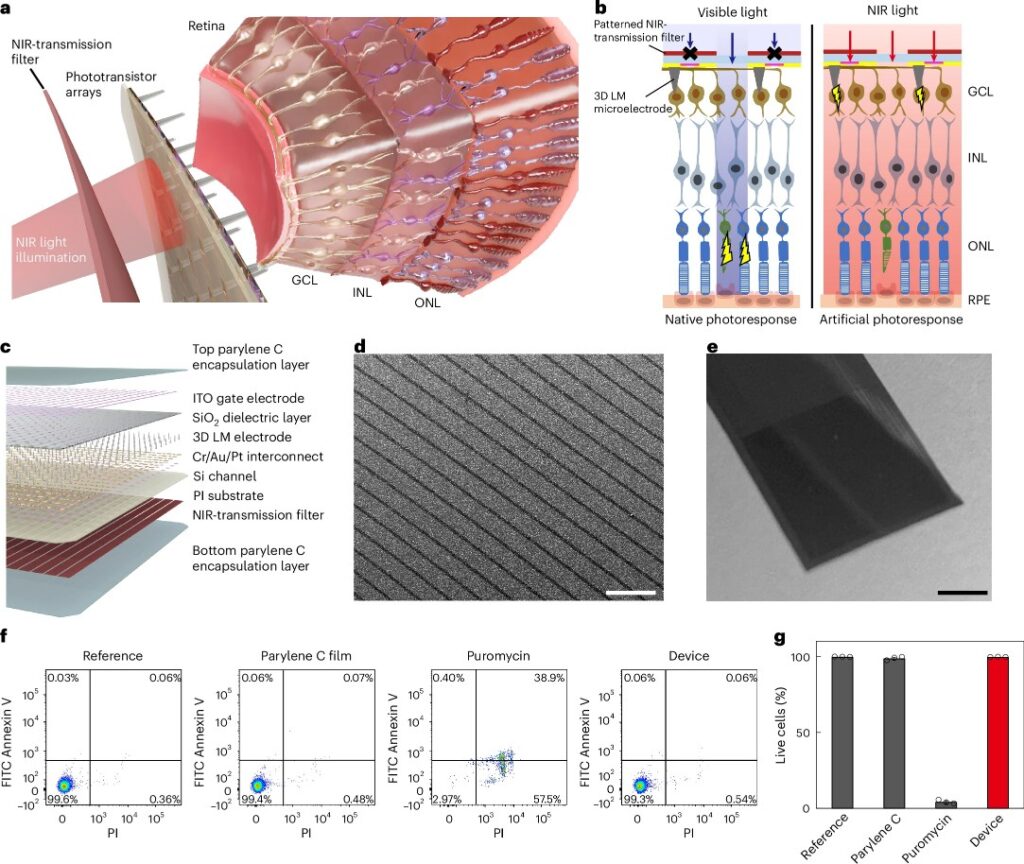
Tre strati e un’idea: filtro, fototransistor, metallo liquido
Il dispositivo è composto da tre elementi. In cima, un filtro ultrasottile che blocca la luce visibile e lascia passare solo l’infrarosso. Sotto, una griglia di fototransistor (sensori microscopici che trasformano la luce in corrente). Alla base, una serie di micropillar, piccoli elettrodi alti circa sessanta micrometri e larghi venti, che entrano in contatto diretto con le cellule gangliari.
Il dettaglio meno scontato sono proprio i micropillar. Sono fatti di una lega di gallio e indio, due metalli che a temperatura ambiente sono liquidi. La loro morbidezza si avvicina a quella del tessuto biologico molto più di qualunque elettrodo rigido. Risultato: meno danno meccanico, meno infiammazione, contatto più stabile sulla superficie curva e irregolare della retina.
Tre prove, tre risposte
I ricercatori hanno testato questa retina artificiale a livelli diversi. Prima sulle retine isolate, fuori dal corpo. Le cellule gangliari di topi sani hanno reagito alla luce blu, come previsto, e non all’infrarosso. Quando il dispositivo è stato attivato, l’infrarosso ha cominciato a generare segnali nervosi paragonabili per intensità a quelli prodotti dalla luce visibile in retine sane. Lo stesso effetto si è visto su retine degenerate.
Secondo passaggio: impianto in topi vivi, con sonde nella corteccia visiva primaria. Prima dell’impianto, i topi ciechi non rispondevano significativamente né al visibile né all’infrarosso. Dopo l’impianto, l’infrarosso ha prodotto attività cerebrale chiara nell’area che elabora la vista. Nei topi sani, la corteccia continuava a rispondere alla luce visibile attraverso i fotorecettori naturali, e si accendeva anche per l’infrarosso quando il dispositivo era acceso. Due canali distinti, paralleli, che non si pestavano i piedi.
Terzo passaggio: il comportamento. I topi sono stati addestrati a leccare quando una luce annunciava l’arrivo dell’acqua. Quelli ciechi con impianto hanno iniziato a leccare in anticipo, non appena si accendeva l’infrarosso. Quelli ciechi senza impianto, no. I topi sani con impianto reagivano sia alla luce visibile che all’infrarosso, con risposte più decise quando l’intensità saliva.
Il punto: un canale aggiunto, non sostituito
Qui sta la differenza con quasi tutte le protesi retiniche immaginate finora. Quelle classiche, basate su luce visibile, rischiano di interferire con la poca vista residua di un paziente. Per chi ha una retinite pigmentosa avanzata, anche un fascio di luce sfocata, una sagoma percepita di lato, è un patrimonio che non si vuole perdere. Una protesi che lavora sulla stessa frequenza naturale può sovrascriverlo.
L’infrarosso, invece, gira su un canale che il nostro occhio non usa. Il paziente potrebbe (in linea teorica) tenere la vista residua e aggiungerci una capacità nuova, attivabile soprattutto in condizioni di buio, magari con una sorgente infrarossa dedicata. Un meccanismo di visione notturna, ma incarnato, non appoggiato a un visore esterno.
Dove va a finire una cosa del genere
Park Jang-ung è stato esplicito sulle possibili applicazioni di questa retina artificiale: difesa, sorveglianza notturna, diagnostica medica, interfacce neurali. È una lista che vale la pena rileggere lentamente. La cecità è la porta d’ingresso. Quello che entra, dopo, è un altro paradigma. Una retina artificiale che funziona come add-on sensoriale, non come riparazione.
I dati di sicurezza, per ora, sono incoraggianti. Le cellule dell’epitelio pigmentato retinico umano, coltivate sul materiale del dispositivo, hanno mantenuto un’alta vitalità. Negli impianti sui topi, gli elettrodi sono rimasti in posizione per sei mesi senza segni evidenti di infiammazione, gliosi o attivazione microgliale. Sei mesi sui topi non sono cinque anni su un essere umano, ovviamente.
Retina artificiale, quello che la scienza ancora non sa
Resta una domanda che il paper non risolve, e che probabilmente nessun esperimento sui topi può risolvere. Se un giorno un essere umano riceverà un dispositivo del genere, come apparirà l’infrarosso al suo cervello? Un colore impossibile? Un lampo? Una forma di luminosità senza tinta? Una sensazione completamente nuova, che dovremo imparare a nominare?
I nostri sensi non sono solo recettori. Sono linguaggi. Aggiungere un canale sensoriale a un cervello adulto significa, prima ancora che vedere qualcosa di nuovo, costruirsi le parole per dire cosa si sta vedendo. La risposta, se mai arriverà, non sarà un grafico in un articolo scientifico.
Sarà il racconto della prima persona che, dopo l’impianto, proverà a descrivere quello che il resto del mondo non vede.


