La tecnologia del vaccino mRNA è nata per il cancro, non per il Covid. BioNTech ci lavorava da prima della pandemia: poi il virus ha preso la scena, i brevetti, i miliardi, gli errori e le polemiche, quelle sbagliate ed anche quelle giuste. Adesso che il mondo si è ripreso da quella mazzata ed è preoccupato per altri problemi, l’azienda di Mainz è tornata al piano originale.
E lo ha fatto in grande: quattro candidati in Fase 3 contemporaneamente, contro melanoma, tumori testa-collo, cancro al pancreas e alla prostata. I primi dati definitivi sono attesi entro fine 2026. Se anche solo due di questi trial centreranno l’obiettivo, l’oncologia cambierà faccia.
Quattro vaccini mRNA, un anno per decidere tutto
Proviamo a capire di cosa stiamo parlando. Il vaccino mRNA contro il cancro non si dichiara come quello per il Covid: non vuole prevenire nulla. È una terapia vera e propria. Il principio è insegnare al sistema immunitario a riconoscere le cellule tumorali come nemiche, fornendogli un identikit molecolare preciso. Un po’ come dare a un detective una foto segnaletica perfetta, invece di dirgli “cerca uno alto”.
BioNTech ha in Fase 3 quattro candidati diversi, ciascuno con una strategia specifica. BNT111 prende di mira il melanoma usando quattro antigeni comuni a oltre il 90% dei tumori cutanei: è un vaccino mRNA “a scaffale”, uguale per tutti i pazienti. BNT113 attacca i tumori testa-collo legati all’HPV, puntando sulle proteine virali che mantengono attivo il tumore. BNT112 affronta il cancro alla prostata, un tumore storicamente “freddo” (cioè quasi invisibile al sistema immunitario) e prova a renderlo “caldo”. E poi c’è BNT122, che è un’altra cosa ancora.

Il vaccino mRNA cucito addosso al paziente
BNT122 (il nome tecnico è autogene cevumeran) è il candidato più ambizioso. Funziona così: si prende un campione del tumore del paziente, si sequenzia il genoma per identificare fino a 20 mutazioni uniche, e si costruisce un vaccino mRNA personalizzato che contiene le istruzioni per produrre esattamente quelle proteine tumorali. Il sistema immunitario le riconosce come estranee e impara a cercarle e distruggerle. La Fase 3 è focalizzata sull’adenocarcinoma pancreatico, uno dei tumori con il tasso di sopravvivenza più basso in assoluto.
Il problema? Costruire un vaccino mRNA da zero per ogni singolo paziente richiede tempo: circa sei settimane dal prelievo alla somministrazione. BioNTech ha automatizzato gran parte del processo e ha sviluppato i BioNTainer, unità di produzione modulari (in pratica container attrezzati come camere sterili) che possono fabbricare il vaccino ovunque nel mondo. Ingegneria logistica, oltre che molecolare.
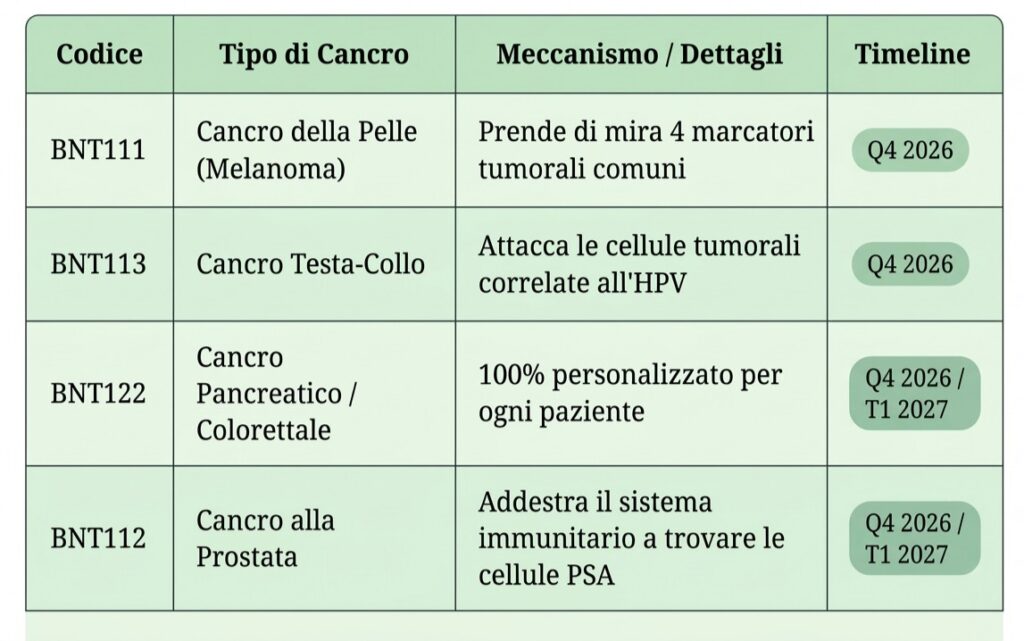
I quattro vaccini mRNA in Fase 3
- BNT111 (melanoma): vaccino “a scaffale”, 4 antigeni tumorali + cemiplimab. Dati attesi: Q4 2026
- BNT113 (testa-collo HPV+): proteine E6/E7 + pembrolizumab. Trial AHEAD-MERIT, dati: Q4 2026
- BNT122 (pancreas/colon-retto): personalizzato, fino a 20 neoantigeni. Dati: Q4 2026 / Q1 2027
- BNT112 (prostata): 5 antigeni prostatici + terapia anti-androgenica. Dati: Q4 2026 / Q1 2027
I dati che già ci sono (e quelli che mancano)
Allora: la base scientifica c’è. I dati a cinque anni sul vaccino mRNA di Moderna/Merck per il melanoma (un prodotto diverso, ma con logica simile) mostrano una riduzione del 49% del rischio di recidiva rispetto alla sola immunoterapia. Cinque anni di follow-up in oncologia sono un segnale forte, soprattutto per un trattamento adiuvante. Ma attenzione: quelli sono dati di Fase 2. I trial di Fase 3 di BioNTech devono ancora dimostrare efficacia su numeri molto più grandi e in contesti clinici diversi.
Il contesto, peraltro, non aiuta. L’amministrazione americana, ad esempio, ha tagliato 500 milioni di dollari di finanziamenti alla ricerca sui vaccini mRNA negli Stati Uniti. BioNTech è tedesca e può procedere, ma l’ecosistema globale della ricerca oncologica ne risente. Sono oltre 230 i trial clinici su vaccini mRNA oncologici attualmente in corso nel mondo: rallentarne il finanziamento significa rallentare risposte che servono a milioni di persone.
Cosa cambia davvero (e cosa no)
Lo dico chiaramente: anche se tutti e quattro i trial centrassero l’obiettivo primario, non stiamo parlando di “curare il cancro” nel 2026. Stiamo parlando di dimostrare che il vaccino mRNA funziona come terapia adiuvante, cioè dopo l’intervento chirurgico, per ridurre il rischio che il tumore torni. È un passo enorme (specie per il pancreas, dove la recidiva è quasi una certezza) ma non è una cura universale. È una potentissima arma in più in un arsenale che ne ha disperatamente bisogno.
I costi restano un problema serio. Un vaccino mRNA personalizzato richiede sequenziamento genomico, produzione individuale e logistica dedicata. Chi lo pagherà? E chi ci avrà accesso? Sono domande che nessun trial clinico può risolvere, e che decideranno quanto questa tecnologia cambierà davvero la vita delle persone (non solo quella dei pazienti nei centri di eccellenza).
Quando e come ci cambierà la vita
Se i risultati di Fase 3 saranno positivi, le prime richieste di approvazione regolatoria (FDA e EMA) potrebbero arrivare nel 2027-2028. I vaccini mRNA “a scaffale” (come BNT111 per il melanoma) avrebbero un percorso più rapido e costi più contenuti. Quelli personalizzati (come BNT122 per il pancreas) richiederanno infrastrutture dedicate e modelli di accesso ancora tutti da inventare.
Per i pazienti, potrebbe significare passare da “operazione + chemio + speranza” a “operazione + vaccino mRNA + immunoterapia + dati concreti sulla riduzione delle recidive”.
Approfondisci
Ti interessa il vaccino mRNA contro il cancro? Leggi anche come i vaccini mRNA sono passati dal Covid all’oncologia. Oppure scopri i trial clinici BioNTech sul cancro del colon-retto per capire da dove è partita la Fase 2.
BioNTech ha iniziato a lavorare sui vaccini mRNA contro il cancro quasi 20 anni fa, nel 2008. Ha impiegato quindici anni per arrivare alla Fase 3, e nel mezzo ha fatto una “deviazione” che ha cambiato il mondo.
Adesso è tornata al punto di partenza, con quattro trial aperti e un anno per dimostrare che l’idea originale funzionava. Nessuno sa ancora come andrà a finire, ma per la prima volta la risposta arriverà dai dati e non dalle promesse.
E nel mondo dell’oncologia, i dati sono l’unica moneta che conta.


